Сахароза — Википедия
Материал из Википедии — свободной энциклопедии
Перейти к навигации Перейти к поиску Эта статья — о химическом веществе. О пищевом продукте см. Сахар.| Сахароза | |
|---|---|
| Систематическое наименование | (2R,3R,4S,5S,6R)-2-[(2S,3S,4S,5R)-3,4-дигидрокси-2,5-бис(гидроксиметил)оксолан-2-ил]окси-6-(гидроксиметил)оксан-3,4,5-триол |
| Традиционные названия | α-D-глюкопиранозил-β-D-фруктофуранозид, свекловичный сахар, тростниковый сахар |
| Хим. формула | C12H22O11 |
| Состояние | Твёрдое, кристаллическое |
| Молярная масса | 342,2965 ± 0,0144 г/моль |
| Плотность | 1,587 г/см³ |
| Т. плав. | 186 °C |
| 367 ± 1 °F[1] и 320 ± 1 °F[1] | |
| Давление пара | 0 ± 1 мм рт.ст.[1] |
| Растворимость в воде | 211,5 |
ru.wikipedia.org
Какова формула сахара, соли, воды, спирта, уксуса и прочих веществ?
Химические формулы распространённых в быту веществ полезно знать не только как часть школьного курса химии, но и просто для общей эрудиции. Формулу воды или поваренной соли знают практически все, однако насчёт спирта, сахара или уксуса — немногие смогут сразу попасть в точку. Давайте пойдём от простого к сложному.
Какова формула воды?
Эту жидкость, благодаря которой на планете Земля появилась удивительная живая природа, знают и пьют все. Более того, она составляет около 70% нашего с вами тела. Вода является простейшим соединением атома кислорода с двумя атомами водорода.
Химическая формула воды: H2O
Какова формула поваренной соли?
Поваренная соль является не только незаменимым кулинарным блюдом, но и одной из главных составляющих морской соли, запасы которой в Мировом Океане составляют миллионы тонн. Формула поваренной соли проста и легка для запоминания: 1 атом натрия и 1 атом хлора.
Химическая формула поваренной соли: NaCl
Какова формула сахара?
Сахар — белый кристаллический порошок, без которого ни один сладкоежка в мире не сможет прожить и дня. Сахар является сложным органическим соединением, формулу которого сразу не запомнишь: 12 атомов углерода, 22 атома водорода и 11 атомов кислорода образуют сладкую и сложную структуру.
Химическая формула сахара: C12H22O11
Какова формула уксуса?
Уксус — раствор уксусной кислоты, который используют в пищу, а также для очистки металлов от налёта. Молекула уксусной кислоты имеет сложную структуру, состоящую из двух атомов углерода, к одному из которых крепятся три атома водорода, а к другому — два атома кислорода, один из которых прихватил себе ещё один водород.
Химическая формула уксусной кислоты: CH3COOH
Какова формула спирта?
Начнём с того, что спирты бывают разные. Тот спирт, что используется для приготовления вин, водки и коньяков, называется по-научному этанол. Помимо этанола есть ещё куча спиртов, которые используются в медицине, автомобилестроении и авиации.
Химическая формула этанола: C2H5OH
Какова формула пищевой соды?
Пищевая сода называется по-научному гидрокарбонатом натрия. Из этого названия любой начинающий химик поймёт, что в молекуле соды есть натрий, углерод, кислород и водород.
Химическая формула пищевой соды: NaHCO3
Сегодня 6 августа 2019 года. А вы знаете, какой сегодня праздник?
| Оцените качество ответа: |
Рекомендуем также почитать:
navopros.ru
Алгоритм выполнения лабораторной работы по химии в 8 классе «Приготовление раствора сахара с массовой долей вещества»
Урок — лабораторная работа в 8 классе.
Тема: «Приготовление раствора сахара с заданной
Цель работы:
-отработать навык рассчитывать массовую долю вещества в растворе и уметь готовить такие растворы на практике;
-отработать практические навыки взвешивания вещества, определения объема вещества, растворения;
-осуществление межпредметных связей между химией, математикой и физикой;
— приобретение практических навыков и знаний необходимых в повседневной жизни.
Оборудование и реактивы: весы с разновесами, колба коническая, стаканчик с сахарным песком, палочка, колба с водой, мерный цилиндр.
Ход урока:
Повторить с учащимися технику безопасности в кабинете химии.
Проводите опыты по указанию учителя, соблюдая правила безопасности.
Для опыта берите вещества в указанных количествах.
Наливайте и насыпайте реактив только над столом.
Пролитые или рассыпанные реактивы немедленно удалите по указанию учителя.
II. В кабинете химии запрещается:
1. Пробовать вещества на вкус, есть, пить.
2. Оставлять открытыми склянки с жидкостями и банки с сухими реактивами, наклоняться над склянками с реактивами.
3. Делать глубокий вдох, определяя летучее вещество по запаху.
4. Сливать или ссыпать оставшиеся вещества в сосуд, из которого они взяты.
Класс делится на группы (1 вариант и 2 вариант у учащихся).
Задание 1 уровня. (Задание для 1 группы, написанные на карточках)
Приготовьте 200мл 10% раствора поваренной соли.
Алгоритм работы.
Рассчитайте массу солсахара, необходимой для приготовления данного раствора, по формуле:
m(в-ва)= m(раствора) W \ 100%
Рассчитайте массу воды, необходимую для приготовления раствора:
m(воды) = m(р-ра) — m(в-ва)
Рассчитайте объем воды, если плотность воды равна 1г\мл (1кг\м3)
Взвесьте на весах необходимое количество сахара.
Измерьте мерным цилиндром необходимое количество воды.
Смешайте в колбе сахар и воду.
Сделайте вывод.
Наведите порядок на своем рабочем месте.
Задание 2 уровня. (Задание для 2 группы, написанные на карточках)
Приготовьте раствор сахара массой 150г и с массовой долей 0,1.
Алгоритм работы.
Выберите, какие формулы, и в какой последовательности вам понадобятся для решения данной задачи:
Вычислите по формулам массу вещества ( сахара ), которая понадобится для получения вашего раствора.
W%= m(в-ва) * 100% \ m(р-ра)
Отмерьте мерным цилиндром нужный объем воды.
Приготовьте раствор в колбе.
Сделайте вывод.
Наведите порядок на своем рабочем месте.
Оформите практическую работу в тетради.
Итог урока.
infourok.ru
Сахароза — урок. Химия, 8–9 класс.
Дисахариды — углеводы, при гидролизе которых их молекула распадается на две молекулы моносахаридов.
Общая формула дисахаридов — C12h32O11. Наиболее известный дисахарид — сахароза, или свекловичный сахар.
Сахароза широко распространена в растительном мире. Она содержится в соке всех растений. Особенно много её в корнеплодах сахарной свёклы, в стеблях сахарного тростника, в соке сахарного клёна. Эти растения специально выращивают, чтобы получать из них сахарозу.
Сахарный тростник
Сахарная свёкла
Сахароза — кристаллическое вещество, хорошо растворимое в воде, сладкое на вкус.
Она подвергается гидролизу, т. е. разложению водой. Если к раствору сахарозы добавить раствор серной кислоты и смесь прокипятить, то образуется смесь двух моносахаридов — глюкозы и фруктозы. Поэтому сахарозу относят к дисахаридам.
C12h32O11+h3O→C6h22O6+C6h22O6.
При нагревании сахароза легко плавится, обугливается, но не горит. Смесь же сахарной пыли с воздухом может взрываться.
Применяется сахароза в питании для придания продуктам сладкого вкуса. В организме она расщепляется на глюкозу и фруктозу и в таком виде затем усваивается.
Употребление слишком большого количества сахара может привести к серьёзным нарушениям обмена веществ и вызвать сахарный диабет.
Источники:
Рудзитис Г. Е., Фельдман Ф. Г. Химия. 9 класс. М.: Просвещение, 2009. — 169 с.
Габриелян О. С. Химия. 9 класс. Учебник для общеобразовательных учреждений. М.: Дрофа, 2011. — 232 с.
www.yaklass.ru
Урок по химии 8 класс
Урок химии в 8 классе «Химия. Здоровье. Красота.»
Пояснительная записка.
Цели: расширение представлений, учащихся о веществах, развитие их интереса к познанию химии, демонстрации ее значения в жизни современного общества и роли потребностей человечества в становлении и развитии химической науки, повышения общего уровня культуры учащихся.
Задачи.
Образовательные: 1. Сформировать представление учащихся о качестве потребляемых продуктов и правильном выборе.
Развивающие: Способствовать формированию умений: наблюдать, анализировать, делать выводы.
Воспитательные: Способствовать воспитанию интереса к предмету, установлению связей теоретического материала с жизнью.
В ходе урока используется следующее оборудование
Тип урока: интегрированный урок с элементами компьютерной технологии, проектной деятельности.
Методы: практический (исследовательски-творческий).
Ход урока.
Учитель. Что такое здоровье и что такое красота, знают все. Всем также известно, насколько полезны для нашего организма яблоки и мед. А что такое химия? Часто мы слышим: «Там же одна химия!» Неужели химия приносит только вред? Конечно же нет! Сегодня мы рассмотрим яблоки и мед с химической точки зрения, поговорим об их химическом составе и воздействии на организм человека.
Запишите тему урока: «Химия. Здоровье. Красота».
Ведущий 1. На определенном этапе развития науки всестороннему изучению были подвергнуты яблоки. Ученые исследовали их химический состав и воздействие на организм человека. Об этом нам расскажут специалисты в области медицины и биохимии.
Биохимик 1. В специализированных лабораториях по изучению биоактивных веществ был изучен химический состав яблок. И вот что было установлено. В любом яблоке есть витамины В1, В2, В5, РР, С, К, Е, Р, каротин. Витамин Е в сочетании с витаминами А и С помогает организму успешно противостоять раковым заболеваниям. Витамин РР оказывает укрепляющее действие на капилляры. В нем нуждаются люди, страдающие гипертонией. Эксперименты показали, что яблоками с повышенным содержанием этого витамина вполне можно лечить легкие формы гипертонической болезни без каких- либо дополнительных медикаментозных средств.
Врач 1. Хочу добавить, что яблоки с высоким содержанием витамина РР полезны людям с повышенной ломкостью кровеносных сосудов (склерозом)
Пытаясь объяснить снижение смертности от болезней сосудов головного мозга, которое наблюдается в Англии в последние несколько десятилетий, английские ученые выдвинули предположение, что это связано с увеличением потребления свежих фруктов и овощей.
Выяснилось, что ломкость артерий у гипертоников возникает от недостатка в организме витамина РР и аскорбиновой кислоты. Кроме того, большое значение имеет соотношение количеств ионов калия и натрия в клетках. В свежих овощах и фруктах всегда много калия и мало натрия. Натрий, как известно, задерживает воду в организме, а калий, наоборот, способствует снижению повышенного артериального давления. Вот почему увеличение потребления овощей, фруктов, и в частности яблок, можно рассматривать как существенную меру предупреждения болезней сосудов головного мозга.
Учитель. Кстати если есть каждое утро одно яблоко, то продолжительность жизни увеличивается на 17 лет.
Ведущий 1. Однако не только витаминами определяется польза яблок. В яблоках содержатся пектиновые вещества. А что такое пектины и какую роль они играют в нашем организме?
Биохимик. Пектины- это выкомолекулярные углеводы, которые содержатся в клеточном соке. Пектиновые вещества не перевариваются в желудочно-кишечном тракте. Они адсорбируют ядовитые вещества, которые затем выводятся из организма. Именно поэтому сырые тертые яблоки – одно из лучших средств от расстройства желудка. Способствует лечению таких заболеваний наличие в яблоках, особенно в антоновке, антимикробных соединений типа лизоцима.
Ведущий 1. А я знаю, что у пектинов есть еще одно замечательное свойство: они обладают способностью связывать и выводить из организма ядовитые тяжелые металлы.
Врач. Пектины действительно выводят из организма тяжелые металлы – медь, свинец, кобальт. Поэтому яблочная диета полезна людям, которые работают на вредных производствах. например, (в типографиях и т.д.).
Врач 1. В яблоках содержится сбалансированный комплекс сахаров. Глюкоза, фруктоза и сахароза не вызывают перенасыщение крови сахаром, поэтому потребление яблок не противопоказано людям, страдающим сахарным диабетом.
Учитель. Нашими учащимися на факультативных занятиях по Здоровому образу жизни была проведена исследовательская работа, что созревание фруктов представляет собой химический процесс, при котором происходит превращение крахмала в сахар.
Проект № 1
Учитель наша экспертная группа провела исследования самых популярных сортов яблок, продаваемых в наших магазинах.
Проект 2.
Учитель. Мы с вами определим наличие аскорбиновой кислоты в соках разных марок. (Решение задач)
1.Яблочный сок «Моя Семья»
1) Отмеряем 10 мл сока, разбавляем его водой до объёма 100 мл.
Определяем содержание витамина С в соке методом йод метрии.
Расчёты: 1 мл 5 %р-ра иода — 35 мг аскорбиновой кислоты
0,29 мл 5 % р-ра? иода – Х мг аскорбиновой кислоты => Х = 0,29?35 = 10 мг
Яблочный сок «Агуша».
1) Отмеряем 10 мл сока, разбавляем его водой до объёма 100 мл.
Определяем содержание витамина С в соке методом йод метрии.
Расчёты: 1 мл 5 %р-ра иода — 35 мг аскорбиновой кислоты
0,14 мл 5 % р-ра иода – Х мг аскорбиновой кислоты => Х = 0,14?35 = 4.9мг
Яблочный сок «GOLD» («Добрый»).
1) Отмеряем 10 мл сока, разбавляем его водой до объёма 100 мл.
Определяем содержание витамина С в соке методом йод метрии.
Расчёты: 1 мл 5 %р-ра иода — 35 мг аскорбиновой кислоты
0,07 мл 5 % р-ра иода – Х мг аскорбиновой кислоты => Х = 0,07?35 = 2.45 мг
Вывод по эксперименту Исследуя содержание витамина С в нектарах мы выяснили, что больше всего витамина С содержится в Яблочный сок «Сочная долина» (10 мг), Яблочный сок «Агуша» (4,9 мг), как и в Яблочный сок «GOLD» занимает третью позицию (2,45 мг).
Задача. Например, 100 мл сока весит 104 гр., а 100 мл воды весит 100 гр. Удельный вес сока будет: 104 : 100 = 1,040. От удельного веса отнимаем единицу: 1,040 — 1,00 = 0,040, или просто 40 (для упрощения расчетов). Эту разность и делим на 5 и получаем процентное содержание сахара в соке, т. е. 40 : 5 = 8 или 8 %.
Проект Социологический опрос.
Учитель переходим к исследованию второму пищевому компоненту меду.
Врач. Пчелиный мед с незапамятных времен применяется как лечебное средство. Лечебные свойства меда объясняются в основном большим содержанием в нем глюкозы, которая не только высокопитательная, но и повышает защитную функцию печени, тонус сердечно – сосудистой системы и сопротивляемость организма инфекциям.
Мед, легче усваивающийся организмом, чем обычный сахар,- ценный диетический продукт. Известно множество диетических блюд, содержащих мед. Наибольшую ценность из них представляют те, приготовление которых не требует нагревания выше 600С. Например, полезно добавлять мед к различным кашам.
Биохимик. Для определения натуральности и качества меда следует проанализировать три признака: питательность, неизменность природного состава и возможность хранения.
Питательность меда зависит в основном от содержания углеводов и его зрелости, причем зрелость определяет не только пищевые и вкусовые, но и лечебные качества.
Созревание меда — эго ряд биохимических превращений, основу которых составляет ферментативный гидролиз сахарозы и удаление воды.
Говоря о качестве меда, необходимо отметить, что кристаллизация — его естественный процесс. Кристаллизуясь, мед меняет свой цвет. Не кристаллизуются или медленно кристаллизуются падевые меда, подвергшиеся нагреванию, а также некоторые фальсифицированные.
Натуральный цветочный мед обладает приятным запахом. Фальсифицированный мед запаха не имеет. Исключение составляют некоторые цветочные меда, которые обладают еле уловимым запахом.
Проект 3 «Определение качества меда»
Учитель. Натуральный мед, растворенный в воде (1:2), будет слегка мутноват или с радужной игрой цветов. При наличии примесей в меде они выпадут в осадок. Можно добавить к осадку несколько капель уксусной эссенции. Если при этом наблюдается вспенивание (выделяется углекислый газ), то, следовательно, в меде есть примесь мела.
Попробуйте добавить к раствору меда несколько капель настойки йода. Возникновение при соединении синего цвета указывает на присутствие в продукте крахмала или муки.
Если при добавлении к 5-10%-му раствору меда небольшого количества ляписа выпадет осадок, то в меде присутствует тростниковый сахар (сахароза).
Методика определения содержания глюкозы в разных сортах меда
В пробирку налить раствора меда (5 капель меда в 5 мл воды). В стаканчик на 100 мл прилить 10 мл раствора сульфата меди (II) и (при размешивании) 20 мл раствора гидроксида натрия. Затем полученную взвесь гидроксида меди (II) добавить в пробирки с раствором меда при комнатной температуре. Определить время проявления первых признаков реакции.
Как установить примеси в меде.
Для этого в небольшую пробирку помещают пробу меда (желательно со дна посуды) и добавляют немного дистиллированной воды. После растворения меда в осадке проявится примесь (например, сахарная пыль).
Крахмальная примесь в меде обнаруживается путем добавления к разбавленной дистиллированной водой пробе нескольких капель йода. Реакция покажет синее окрашивание раствора.
Если в меде содержится мел, то при прибавлении к раствору меда нескольких капель какой-либо кислоты или уксуса произойдет вскипание вследствие выделения углекислого газа.
Примесь сахарной патоки к меду определяют путем добавления к 5-10%-ному раствору пробы азотнокислого серебра (или ляписа). В результате получается белый осадок хлористого серебра. В чистом меде осадка нет. Можно действовать и другим способом. К 5 см3 раствора меда на дистиллированной воде прибавляется 2,5 г свинцового уксуса и 22,5 см3 метилового (древесного) спирта. Образовавшийся обильный желтовато-белый осадок указывает на присутствие сахарной патоки в меде.
Проверьте, добавлены ли в мед вода и сахар
Для этого на лист низкосортной бумаги, которая хорошо впитывает влагу, капните мед. Если он растечется по бумаге, образуя влажные пятна, или даже просочится сквозь нее — это фальшивый мед.
Узнайте, есть ли в меде другие примеси Для этого возьмите раскаленную проволочку (из нержавейки) и опустите ее в мед. Если на ней повиснет клейкая инородная масса — перед вами подделка под мед, если же проволочка останется чистой — мед натуральный или, другими словами, полноценный
Учитель демонстрирует опыт «Определение глюкозы в различных сортах меда». Учащиеся проводят с раствором меда.
Инструкция
Налейте в пробирку 1 мл раствора гидроксида натрия.
Добавьте 2-3 капли раствора сульфата меди (ІІ).
Добавьте несколько капель яблочного сока или раствора меда. Что наблюдаете?
Осторожно нагрейте содержимое пробирки. Что наблюдаете?
Определение содержания глюкозы в разных сортах меда (приложение 4)
№ п/п
Наблюдения
Выводы
1
Мгновенная реакция. Выпал ярко-синий осадок
Данный образец меда в большом количестве содержит природную глюкозу, содержащуюся в нектаре цветов
2
Выпал ярко синий осадок через 4 минуты после начала реакции.
Данный образец меда содержит меньшее количество глюкозы, чем предыдущий, т.к. реакция протекала медленнее
3
Выпал ярко-синий осадок через 9 минут
Данный образец меда, вероятно, содержит в своем составе примеси сахара, т.к. первые признаки протекания реакции начали проявляться только спустя 9 минут. Это время необходимо для того, чтобы произошел щелочной гидролиз дисахарида, а образующийся в результате этой реакции сахар мог вступить в реакцию с Сu(OH)2
4
Мгновенная реакция. Выпал ярко-синий осадок
Данный образец меда в большом количестве содержит природную глюкозу, содержащуюся в нектаре цветков липы
5
Выпал ярко-синий осадок через 11 минут после начала реакции
Данный образец меда, вероятно, содержит в своем составе примеси сахара, т.к. первые признаки протекания реакции начали проявляться только спустя 11 минут. Это время необходимо для того, чтобы произошел щелочной гидролиз дисахарида, а образующийся в результате этой реакции сахар мог вступить в реакцию с Сu(OH)2
Ведущий 1. Яблоки и мед используются в косметологии.
Косметолог. С удовольствием рекомендую своим пациентам маски с использованием яблок. Наибольший эффект они оказывают после горячего компресса или паровой ванны. Время действия масок обычно ограничивают 15- 30 мин. После наложения маски необходимо расслабиться, лицо должно быть неподвижным и спокойным. Снимают маску легко, без усилий, не растягивая кожу. После процедуры обязательно протирают кожу лосьоном или смазывают кремом, соответствующим типу кожи. Достаточно делать маски 1-2 раза в неделю. Курс может составлять 15- 20 процедур, при необходимости его можно повторить через 1,5 –2 месяца. Мед в комплексе с другими веществами хорошо укрепляет и смягчает кожу, устраняет сухость и шелушение, делает кожу нежной и гладкой. Предлагаю рецепты питательных масок.
Буклет №1.
Ведущий 1. Думаю, теперь самое время предоставить слово нашим кулинарам и кондитерам. Они расскажут, какие напитки, выпечку и салаты можно приготовить из яблок и меда.
Буклет №2.
Кулинар демонстрирует приготовление коктейля.
Кондитер. Спору нет, употребление сладких и мучных блюд необходимо резко ограничивать, особенно тем, кто склонен к полноте.
Однако трудно представить себе воскресный обед или праздничный ужин без пирогов, тортов, пирожных, пряников, печенья…. Поделюсь с вами несколькими рецептами приготовления сладостей с использованием яблок и меда. Несомненно, эти блюда понравятся вам и вашим близким.
Кулинар. Предлагаю несколько рецептов коктейлей и салатов красоты. Они получили такое название за свои удивительные свойства – регулярное их употребление в пищу придает лицу великолепный здоровый цвет, не говоря уже о том, что минеральные соли, витамины, входящие в состав коктейлей и салатов, улучшают жизнедеятельность всего организма.
Учитель. Вами была проведена большая работа и я надеюсь, что все наши советы будут вами учтены и приняты во внимание. На этом наш урок окончен, желаю всем отличного здоровья.
infourok.ru
Формула сахара по химии
Определение и формула сахара
Формула –
На долю углеводов приходится около сухого вещества растений и около животных.
Растения синтезируют углеводы из неорганических соединений: и .
Классификация сахаров
Углеводы делятся на две группы:
- Моносахариды (монозы)
- Полисахариды (полиозы), которые подразделяются на сахароподобные (олигосахариды), к которым относятся дисахариды (биозы), трисахариды и несахароподобные полисахариды.
Моносахариды
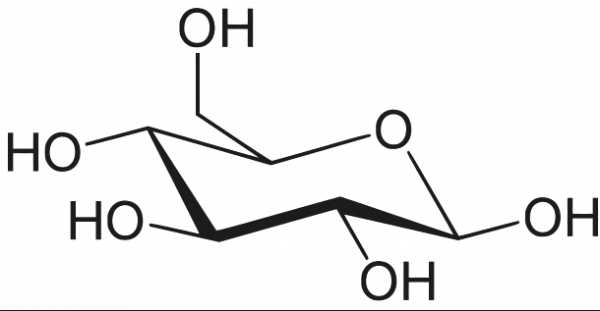
В природе наиболее распространено два вида моноз: пентозы и гексозы .
Одни монозы ведут себя как гидроксиальдегиды (альдозы), другие — как гидроксикетоны (кетозы).
Одни монозы ведут себя как гидроксиальдегиды (альдозы), другие — как гидроксикетоны (кетозы).
Наиболее часто встречаются два моносахарида: глюкоза (альдоза) и фруктоза (кетоза).
Дисахариды
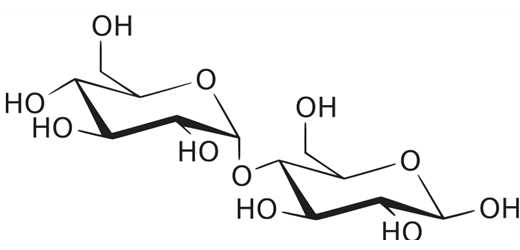
Дисахариды при гидролизе образуют два одинаковых или разных моносахарида.
Их можно разделить на восстанавливающие и невосстанавливающие.
Полисахариды
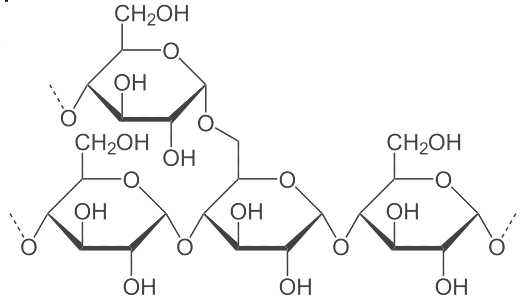
Два самых важных полисахарида — это крахмал и клетчатка (целлюлоза) — построены из остатков глюкозы.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
План-конспект урока по химии (8 класс) на тему: Урок химии в 8 классе в школе I,II вида. Практическая работа «Описание физических свойств веществ» (конспект, презентация)
Тема: Практическая работа №3 «Описание физических свойств веществ»
Цель урока:
- познакомить учащихся с различными образцами веществ, описать их физические свойства
Задачи:
Образовательные:
- совершенствовать знания о физических свойствах веществ;
- совершенствовать экспериментальные умения;
- соблюдать правила техники безопасности.
Развивающие:
- совершенствовать умения применять знания и практические умения, работая по инструкции; наблюдать и фиксировать наблюдения
- развивать познавательную активность учащихся, расширять их кругозор, вырабатывать умение анализировать, делать выводы;
- устанавливать межпредметные связи, формировать мировоззренческие понятия о познаваемости природы.
- раскрыть причинно-следственную связь между строением вещества и его свойствами.
Воспитательные:
- воспитывать умение высказывать собственное мнение, сотрудничать в группе;
- создать условия для развития познавательного интереса к предмету.
Коррекционные:
- контролировать произношение и развивать речь учащихся;
- работать над пополнением предметного словаря;
- развивать остаточный слух учащихся.
Словарь: агрегатное состояние, цвет, блеск, запах, твердость, растворимость, плотность, хрупкость, пластичность.
Оборудование и реактивы: штатив с пробирками, стеклянная палочка, кусочек стекла, образцы веществ: железо (гвоздь), медь, графит, вода, нашатырный спирт, поваренная соль, сахар, мел, медный купорос, алюминий, песок и т. д.
Ход урока
- Организационный момент.
- Проверка ЗУА.
2. Знакомство с темой урока.
— Сегодня у нас практическая работа. Тема работы:«Описание физических свойств веществ». (Слайд)
Цель работы: познакомиться с различными веществами и описать их физические свойства. (Слайд)
— Заполнение протокола: ФИ, класс, дата, цель.
- Речевая работа.
- На этой неделе у вас дежурные звуки И-Э, И –У. Старайтесь их говорить их правильно.
Словарные слова.
— Давайте прочтем словарные слова, которые встретятся на сегодняшнем уроке (Слайд)
- Работа над темой урока.
- Повторение правил ТБ.
— Ребята, вспомним правила, которые нам надо соблюдать при выполнении сегодняшней работы. (Слайд)
- Цель практической работы: познакомиться с некоторыми веществами и изучить их физические свойства
- Инструкция по выполнению работы.
— вам розданы образцы веществ: железо (гвоздь), графит, вода, поваренная соль, нашатырный спирт, медный купорос, мел, кусочек стекла, песок и т. д.
(Слайд)
— Вы должны по плану описать физические свойства веществ (Слайд)
— Свои наблюдения и табличные данные занесите в протокол.
- Выполнение практической работы учащимися.
- Заполнение протокола.
- Задания для контроля.
Задание № 1 . Знакомство со свойствами уксусной кислоты. (Слайд)
Задание №2. (Слайд) Самостоятельная работа.
- Итог урока.
- Какова была тема сегодняшнего урока?
- Что вы делали на практической работе?
- Что вы узнали нового?
- Вы работали….., говорили….
- Домашнее задание.
Оформить протокол, выполнить задания для контроля, написать вывод.
nsportal.ru
